Прорыв в терапии рака
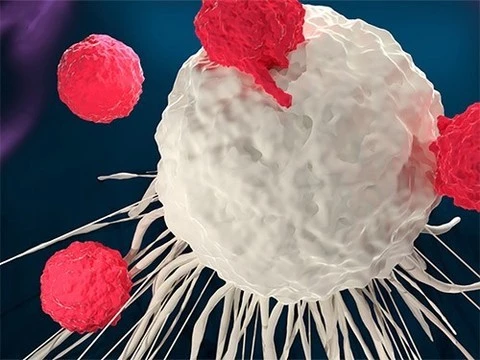
Российские ученые прокомментировали открытие лауреатов Нобелевской премии 2018 года по медицине и физиологии. Новаторские исследования в области лечения рака создали новую область знаний в онкологии и стали пусковым механизмом для создания новых лекарств. Однако эффективно применять его в клинической практике можно будет, только перейдя к персонализированной иммуноонкологии, считают эксперты.
Что это такое и в чем новизна методики
Открытие терапии онкозаболеваний с непростой для восприятия неспециалистом формулировкой «путем ингибирования негативной иммунной регуляции» обсуждалось в рамках университетского проекта NobelTаlks @SechenovUniversity.
Если коротко, то нынешние нобелевские лауреаты изучили способность иммунной системы уничтожать опухолевые клетки, «спуская с цепи» определенные иммунные клетки. В частности, Джеймс Элиссон в 1995 году обнаружил белок CTLA-4, который представляет собой своего рода «тормоз» для клеток иммунной системы (Т-лимфоцитов). В норме это нужно для того, чтобы лимфоциты не атаковали собственные клетки организма. Уже в следующем году, возглавляемая Элиссоном группа научилась выключать этот белок специальными антителами. В результате этого лечения наша иммунная система начинает более активно бороться с опухолевыми клетками.
Несколькими годами ранее Тасуку Хондзе заинтересовал другой белок, PD-1. Он тоже влияет на готовность иммунной системы сражаться с опухолью и был открыт группой Хондзе на поверхности Т-лимфоцитов. Значение этого белка состоит в том, что раковые клетки умеют его блокировать, что мгновенно делает их невидимыми для иммунной системы. Благодаря открытию были разработаны специальные лекарственные препараты, которые нарушают способность опухолевых клеток блокировать PD-1. Это возвращает организму способность видеть и убивать вышедшие из-под контроля опухолевые клетки.
С помощью этого подхода двум группам ученых удалось победить несколько очень распространенных форм рака у мышей. Новый метод уже активно внедряется и применительно к опухолям людей, обещая значительный прорыв в терапии рака.
Подходит не всем
Иммуноонкология – очень перспективное направление, меняющее парадигму лечения многих заболеваний и позволяющее добиться эффекта, не сопоставимого с используемыми сегодня в рутинной практике методами. Важным свойством иммуноонкологических препаратов является универсальность их действия – одна молекула подходит для борьбы с разными видами рака. Так, среди уже зарегистрированных есть препарат сразу для шести различных показаний, в том числе для таких, тяжело поддающихся лечению заболеваний, как немелкоклеточный рак легкого, меланома и рак почки.
Однако на практике иммуноонкологические препараты помогают в борьбе с опухолью далеко не всем: у некоторых пациентов они не дают эффекта, у некоторых, к счастью, в очень небольшом проценте случаев, вызывают взрывоподобный рост опухоли, рассказала проректор по научно-исследовательской работе Сеченовского университета, руководитель Центра персонализированной онкологии OncoTarget Сеченовского университета Марина Секачева.
«Мы находимся в начале пути по изучению эффективности и безопасности этих препаратов, - рассказала Секачева. – Сеченовский университет также активно занимается изучением иммуноонкологии. В Университете идет работа по персонализированному подбору иммуноонкологических препаратов, основываясь на поиске предикторов ответа и эффективности. Перед нами стоит задача найти маркеры, отличительные особенности опухоли и организма, которые позволят предсказать ответ. Только создав подобную стратегию персонализированной иммуноонкологии, мы сможем с максимальной эффективностью применять открытие Нобелевских лауреатов в клинической практике».
Еще один вопрос, на который предстоит ответить ученым: как оптимально сочетать иммуноонкологию с классическими методами противоопухолевого лечения, например, с лучевой терапией. На сегодняшний день накоплено уже много данных по этому вопросу, но все они разрознены. Для обработки этих данных в Университете создана группа «Компьютерная онкология», которая при помощи методик математического моделирования работает над созданием предсказательной модели взаимодействия иммуноонкологических процессов с процессами, происходящими при лучевой терапии.
Когда иммуноонкология станет доступна в России?
Определить категории пациентов, для которых будут эффективны конкретные иммуноонкологические препараты важно и для бюджета, из которого будет финансироваться терапия (сегодня один флакон иммуннологического препарата для онкобольного стоит тысячи долларов, а курс лечения тянет на десятки тысяч). И для самих больных: искусственное «растормаживание» иммунитета всегда связано с риском запустить аутоиммунные заболевания. Понятно, что полностью безвредных лекарств, без побочных действий не существует. Но если при этом новые препараты окажутся еще и неэффективными, это может дискредитировать метод.
По словам работающего с ВОЗ международного эксперта, для определения строго определенных групп пациентов, которым показан этот вид терапии, и уточнения характеристик опухоли необходимо создать систему тестирования пациентов и открыть на территории России специализированные лаборатории. Назначение этой терапии не протестированным пациентам не оправдано, и даже при значительных затратах бюджета, достичь желаемого эффекта не удастся.
 Врачи говорят
Клещевые инфекции — чем опасен анаплазмоз? Объясняет врач
Врачи говорят
Клещевые инфекции — чем опасен анаплазмоз? Объясняет врач







